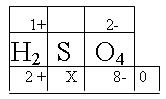Ejercicios Métodos de Balanceo
Balance por Tanteo:
Se emplea para balancear ecuaciones sencillas. Se realiza al "cálculo" tratando de igualar ambos miembros. Para ello utilizaremos el siguiente ejemplo:
Balancear:
N2 + H2 ® NH3
N2 + H2 ® 2 NH3
Balancear:
Al(OH)3 + H2SO4 ® Al2(SO4)3 + H2O
EJERCICIOS
Balancear por Tanteo:
1. Fe + HCl ® FeCl3 + H2
2. H2SO4 + Ca3 (PO4 )2 ® CaSO4 + H3PO4
3. CO2 + H2O ® C6H12O6 + O6
4. C3H8 + O2 ® CO2 + H2O
5. CaCO3 ® CaO + CO2
Se emplea para balancear ecuaciones sencillas. Se realiza al "cálculo" tratando de igualar ambos miembros. Para ello utilizaremos el siguiente ejemplo:
Balancear:
N2 + H2 ® NH3
- Identificamos las sustancias que intervienen en la reacción. En este caso el nitrógeno y el hidrógeno para obtener amoniaco.
- Se verifica si la ecuación está balanceada o no. En este caso notamos que ambos miembros no tienen la misma cantidad de átomos, por lo tanto no está balanceada.
- Se balancea la ecuación colocando coeficientes delante de las fórmulas o símbolos que los necesitan. Empezar con los elementos metálicos o por el que se encuentra presente en menos sustancias:
N2 + H2 ® 2 NH3
- El hidrógeno y oxígeno quedarán para el final. Seguidamente balanceamos el hidrógeno:
- Si un coeficiente no es entero, entonces debe multiplicar todos por el mayor de los denominadores. En este caso no ocurre.
Balancear:
Al(OH)3 + H2SO4 ® Al2(SO4)3 + H2O
- Primero balanceamos el metal aluminio:
- Luego seguimos con el azufre:
- Finalmente continuamos con el hidrógeno, el oxígeno resulta balanceado automáticamente:
EJERCICIOS
Balancear por Tanteo:
1. Fe + HCl ® FeCl3 + H2
2. H2SO4 + Ca3 (PO4 )2 ® CaSO4 + H3PO4
3. CO2 + H2O ® C6H12O6 + O6
4. C3H8 + O2 ® CO2 + H2O
5. CaCO3 ® CaO + CO2
Balanceo por Redox
Recordemos:
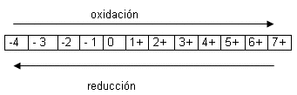
Oxidación: Es un cambio químico, en el cual un átomo o grupo de átomos pierde electrones. En una ecuación química se nota por el aumento algebraico en su estado de oxidación. Ej. :
Al0 ® Al 3+
Reducción: Cambio químico, en el cual un átomo o grupo de átomos gana electrones. En una ecuación química se distingue por la disminución en su estado de oxidación. Ej. :
Fe2+ ® Fe0
Oxidación: Es un cambio químico, en el cual un átomo o grupo de átomos pierde electrones. En una ecuación química se nota por el aumento algebraico en su estado de oxidación. Ej. :
Al0 ® Al 3+
Reducción: Cambio químico, en el cual un átomo o grupo de átomos gana electrones. En una ecuación química se distingue por la disminución en su estado de oxidación. Ej. :
Fe2+ ® Fe0
* Cada salto equivale a un electrón.
Ej. : Si el Al cambia su estado de oxidación de 0 a 3+, significa que ha perdido tres electrones. En cambio el Fe, que ha variado de 2+ a 0, ha ganado dos electrones.
En una reacción química REDOX, la oxidación y la reducción ocurren simultáneamente. El número de electrones ganado por un átomo o grupo de átomos, es perdido por otro átomo o grupo de átomos. En estas reacciones NO hay producción ni consumo de electrones, sólo hay transferencia.
Los elementos que ceden electrones se oxidan y se llaman reductores.
Los elementos que ganan electrones se reducen y se denominan oxidantes.
El número de oxidación, representa el estado de oxidación de un átomo. Permite determinar la cantidad de electrones ganados o perdidos en un cambio químico por un átomo, una molécula o un ión. Se determina de la siguiente manera:
· Los iones simples como Na+ , Ca2+ , S2-, etc. , tienen un número de oxidación idéntico a su carga ( 1+, 2+, 2-), respectivamente.
· Los átomos o moléculas de los elementos libres Fe, Cu, O, P4, Cl2, etc. , tienen número de oxidación 0 (cero), pues no han perdido ni ganado electrones.
· En diferentes compuestos el H y el O tienen número de oxidación 1+ y 2- respectivamente, excepto en los casos en que el hidrógeno forma parte de los hidruros (NaH, LiH...) y el oxígeno forma peróxidos (H2O2...) en ambos casos exhiben número de oxidación 1-; o cuando reacciona con el fluor.
· El número de oxidación de otros átomos en moléculas o iones complejos, se establece así:
· El número de oxidación de los elementos conocidos como el hidrógeno y oxígeno, se escriben en la parte superior en los lugares respectivos. Se multiplica luego por el número de átomos (2*4, 1*2) y los productos se escriben en la parte inferior. La suma total de los números de oxidación de los iones complejos es igual a la carga del ion. En una molécula neutra la suma total es cero; por lo tanto, el número de oxidación del átomo problema se calcula así:
Ej. : Si el Al cambia su estado de oxidación de 0 a 3+, significa que ha perdido tres electrones. En cambio el Fe, que ha variado de 2+ a 0, ha ganado dos electrones.
En una reacción química REDOX, la oxidación y la reducción ocurren simultáneamente. El número de electrones ganado por un átomo o grupo de átomos, es perdido por otro átomo o grupo de átomos. En estas reacciones NO hay producción ni consumo de electrones, sólo hay transferencia.
Los elementos que ceden electrones se oxidan y se llaman reductores.
Los elementos que ganan electrones se reducen y se denominan oxidantes.
El número de oxidación, representa el estado de oxidación de un átomo. Permite determinar la cantidad de electrones ganados o perdidos en un cambio químico por un átomo, una molécula o un ión. Se determina de la siguiente manera:
· Los iones simples como Na+ , Ca2+ , S2-, etc. , tienen un número de oxidación idéntico a su carga ( 1+, 2+, 2-), respectivamente.
· Los átomos o moléculas de los elementos libres Fe, Cu, O, P4, Cl2, etc. , tienen número de oxidación 0 (cero), pues no han perdido ni ganado electrones.
· En diferentes compuestos el H y el O tienen número de oxidación 1+ y 2- respectivamente, excepto en los casos en que el hidrógeno forma parte de los hidruros (NaH, LiH...) y el oxígeno forma peróxidos (H2O2...) en ambos casos exhiben número de oxidación 1-; o cuando reacciona con el fluor.
· El número de oxidación de otros átomos en moléculas o iones complejos, se establece así:
· El número de oxidación de los elementos conocidos como el hidrógeno y oxígeno, se escriben en la parte superior en los lugares respectivos. Se multiplica luego por el número de átomos (2*4, 1*2) y los productos se escriben en la parte inferior. La suma total de los números de oxidación de los iones complejos es igual a la carga del ion. En una molécula neutra la suma total es cero; por lo tanto, el número de oxidación del átomo problema se calcula así:
1+(2) + X + 2-(4) = 0
2 + X + 8- = 0
X = 8 – 2
X = 6
El número encontrado se divide entre el número de átomos problema ( 6/1) y el resultado es el número de oxidación buscado( en este caso del azufre)Balancear:
Al2 O3 + C + Cl2 ® CO + AlCl3
Balancear:
CrI3 + Cl2 + NaOH ® Na2CrO4 + Na I O4 + NaCl + H2O
(Podemos obviar varios pasos):
En este caso especial tres átomos cambian su valencia:
Sumamos las ecuaciones (1 ) y (3 ) para hacer una sola ecuación de oxidación:
Igualamos la cantidad de electrones multiplicando por los factores respectivos: (Por 2 la ec. 4 y por 27 la ec. 5)
Se puede establecer una ecuación básica sumando:
2 CrI3 + 27 Cl2 + ¿ NaOH ® Na2CrO4 + 6 Na I O4 + 54NaCl + ¿ H2O
Completando:
2 CrI3 + 27 Cl2 + 64NaOH ® 2Na2CrO4 + 6 Na I O4 + 54NaCl + 32H2O
(Verificar)
El proceso de oxidación-reducción NO ocurre en las ecuaciones de metátesis. Ej:
NaOH + HCl → NaCl + H2O
EJERCICIOS
Balancear por REDOX:
1. Cu + HNO3 ® Cu(NO3)2 + NO + H2O
2. NaClO3 + K2SnO2 ® NaCl + K2SnO3
3. FeS2 + O2 ® Fe2O3 + SO2
4. Zn + NaNO3 + NaOH ® Na2ZnO2 + NH3 + H2O
5. KMnO4 + H2SO4 + H2O2 ® MnSO4 + O2 + K2SO4
2 + X + 8- = 0
X = 8 – 2
X = 6
El número encontrado se divide entre el número de átomos problema ( 6/1) y el resultado es el número de oxidación buscado( en este caso del azufre)Balancear:
Al2 O3 + C + Cl2 ® CO + AlCl3
- Se determinan los números de oxidación para determinar cambios:
- Se detecta quienes se han oxidado y quienes se han reducido de acuerdo al cambio del número de oxidación:
- Se procede a escribir las ecuaciones iónicas:
- Se multiplica en las ecuaciones el número de electrones por coeficientes adecuados para que el total de electrones perdidos sea igual al número de electrones ganados:
- Se asignan como coeficientes de las sustancias afectadas en la ecuación, los factores que se utilizaron para que el número de electrones sea igual:
- Se concluye el balanceo por tanteo. En el ejemplo como la ecuación ya quedó balanceada, no es necesario este proceso.
Balancear:
CrI3 + Cl2 + NaOH ® Na2CrO4 + Na I O4 + NaCl + H2O
(Podemos obviar varios pasos):
En este caso especial tres átomos cambian su valencia:
Sumamos las ecuaciones (1 ) y (3 ) para hacer una sola ecuación de oxidación:
Igualamos la cantidad de electrones multiplicando por los factores respectivos: (Por 2 la ec. 4 y por 27 la ec. 5)
Se puede establecer una ecuación básica sumando:
2 CrI3 + 27 Cl2 + ¿ NaOH ® Na2CrO4 + 6 Na I O4 + 54NaCl + ¿ H2O
Completando:
2 CrI3 + 27 Cl2 + 64NaOH ® 2Na2CrO4 + 6 Na I O4 + 54NaCl + 32H2O
(Verificar)
El proceso de oxidación-reducción NO ocurre en las ecuaciones de metátesis. Ej:
NaOH + HCl → NaCl + H2O
EJERCICIOS
Balancear por REDOX:
1. Cu + HNO3 ® Cu(NO3)2 + NO + H2O
2. NaClO3 + K2SnO2 ® NaCl + K2SnO3
3. FeS2 + O2 ® Fe2O3 + SO2
4. Zn + NaNO3 + NaOH ® Na2ZnO2 + NH3 + H2O
5. KMnO4 + H2SO4 + H2O2 ® MnSO4 + O2 + K2SO4